Ускорение или замедление химической реакции при изменении температуры является одним из важнейших факторов, влияющих на скорость реакции. Температурный коэффициент скорости реакции представляет собой краткосрочную зависимость скорости химической реакции от температуры.
Факторы влияния на температурный коэффициент скорости реакции могут быть различными, включая энергию активации молекулярных коллизий, изменение термодинамических свойств системы и концентрацию реакционных веществ. Увеличение температуры обычно приводит к увеличению скорости реакции, так как повышается энергия движения молекул и вероятность успешных столкновений.
Понимание температурного коэффициента скорости реакции имеет важное значение в различных областях химии и катализа, так как позволяет предсказать эффективность процессов, происходящих при различных условиях температуры. Изучение этого параметра позволяет оптимизировать условия процессов и повысить их эффективность.
Роль температуры в реакциях
Температура играет ключевую роль в химических реакциях. Все химические реакции происходят при определенной температуре, которая может влиять на скорость и термодинамику реакции.
Повышение температуры обычно увеличивает скорость реакции, так как молекулы имеют большую кинетическую энергию и чаще сталкиваются друг с другом. Это приводит к увеличению вероятности эффективных столкновений молекул, что способствует ускорению процесса реакции.
Также температура может изменять равновесие реакции в зависимости от термодинамических условий. Для некоторых реакций повышение температуры может способствовать обратной реакции, тогда как для других она может сдвинуть равновесие в сторону продуктов.
| Положительные эффекты | Отрицательные эффекты |
|---|---|
| Увеличение скорости реакции | Деградация реагентов или продуктов |
| Изменение равновесия | Повышенное энергопотребление |
Влияние тепла на скорость

Температурный коэффициент скорости реакции (Q) показывает, на сколько изменится скорость реакции при изменении температуры на 10 градусов Цельсия. Q больше 1, что указывает на положительную зависимость между температурой и скоростью реакции.
| Параметр | Влияние на скорость реакции |
|---|---|
| Повышение температуры | Увеличение скорости реакции |
| Понижение температуры | Уменьшение скорости реакции |
Термодинамические аспекты

Температурный коэффициент скорости реакции тесно связан с термодинамическими характеристиками реакций. По умолчанию положительный температурный коэффициент скорости означает, что скорость реакции увеличивается с повышением температуры, так как активационная энергия становится менее критичной.
Активация молекул

При повышении температуры молекулы приобретают большую энергию, что увеличивает их скорость движения и вероятность столкновения, что, в свою очередь, ускоряет реакцию.
| Температура | Повышение температуры ведет к увеличению скорости реакции за счет активации молекул. |
| Катализатор | Катализаторы понижают энергию активации, не изменяя конечную энергетическую барьер. |
Оба эти фактора влияют на скорость химических реакций, и понимание механизмов их действия позволяет оптимизировать процессы и улучшать полученные результаты.
Энергия активации

Энергия активации зависит от конкретной реакции и определяет скорость протекания процесса. Чем ниже энергия активации, тем быстрее реакция происходит. Повышение температуры обычно увеличивает энергию частиц, что способствует преодолению барьера. Энергия активации также зависит от ориентации молекул при столкновении и от наличия катализаторов, способных снизить энергию активации и ускорить реакцию.
Распределение энергий

В химических реакциях энергия распределяется между молекулами в процессе столкновений. По закону сохранения энергии кинетическая энергия частиц при столкновении может переходить во внутреннюю энергию молекул, вызывая изменения их состояния. При увеличении температуры усиливаются коллизии молекул, что способствует более эффективному распределению энергии между реагирующими частицами.
Температурный коэффициент скорости реакции зависит от распределения энергий между молекулами реагентов. С увеличением температуры распределение энергий становится более равномерным, что способствует увеличению числа успешных столкновений и, как следствие, увеличению скорости реакции.
Кинетика реакций
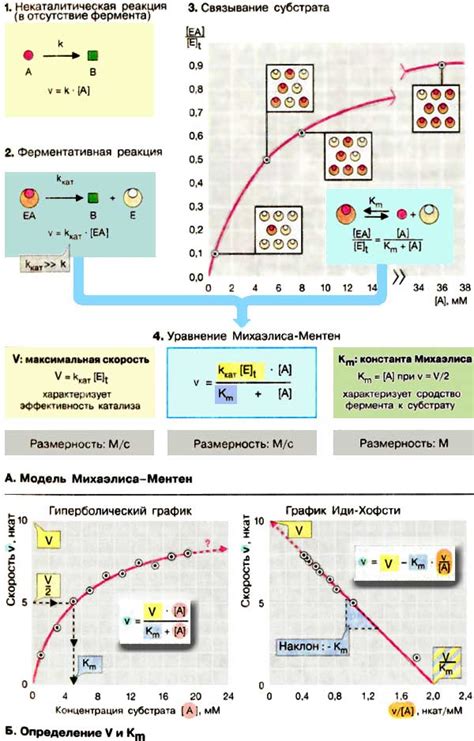
Кинетика реакций изучает скорость химических реакций, факторы, влияющие на эту скорость, и механизмы протекания реакций.
Основными понятиями в кинетике реакций являются скорость реакции, закон скорости реакции, температурные зависимости и активационная энергия.
Изучение кинетики реакций позволяет прогнозировать химические превращения, оптимизировать условия производства и понять механизмы химических процессов.
Вопрос-ответ

Что такое температурный коэффициент скорости реакции?
Температурный коэффициент скорости реакции - это значение, которое показывает, насколько изменится скорость химической реакции при изменении температуры на 1 градус Цельсия. Он определяется как отношение относительного изменения скорости реакции к относительному изменению температуры.
Какие факторы влияют на температурный коэффициент скорости реакции?
На температурный коэффициент скорости реакции влияют несколько факторов. Основные из них это активационная энергия реакции, энергия аррениуса, стохиометрия реакции, концентрация реагентов, а также наличие катализаторов.
Почему при увеличении температуры скорость химической реакции обычно увеличивается?
При увеличении температуры происходит активация молекул реагентов, увеличивается их энергия и частота столкновений. Это приводит к увеличению вероятности успешных столкновений, что в итоге увеличивает скорость химической реакции.
Как изменение температуры влияет на температурный коэффициент скорости реакции?
Изменение температуры влияет на температурный коэффициент скорости реакции следующим образом: при повышении температуры значение коэффициента увеличивается, что означает более быстрое изменение скорости реакции относительно изменения температуры.



